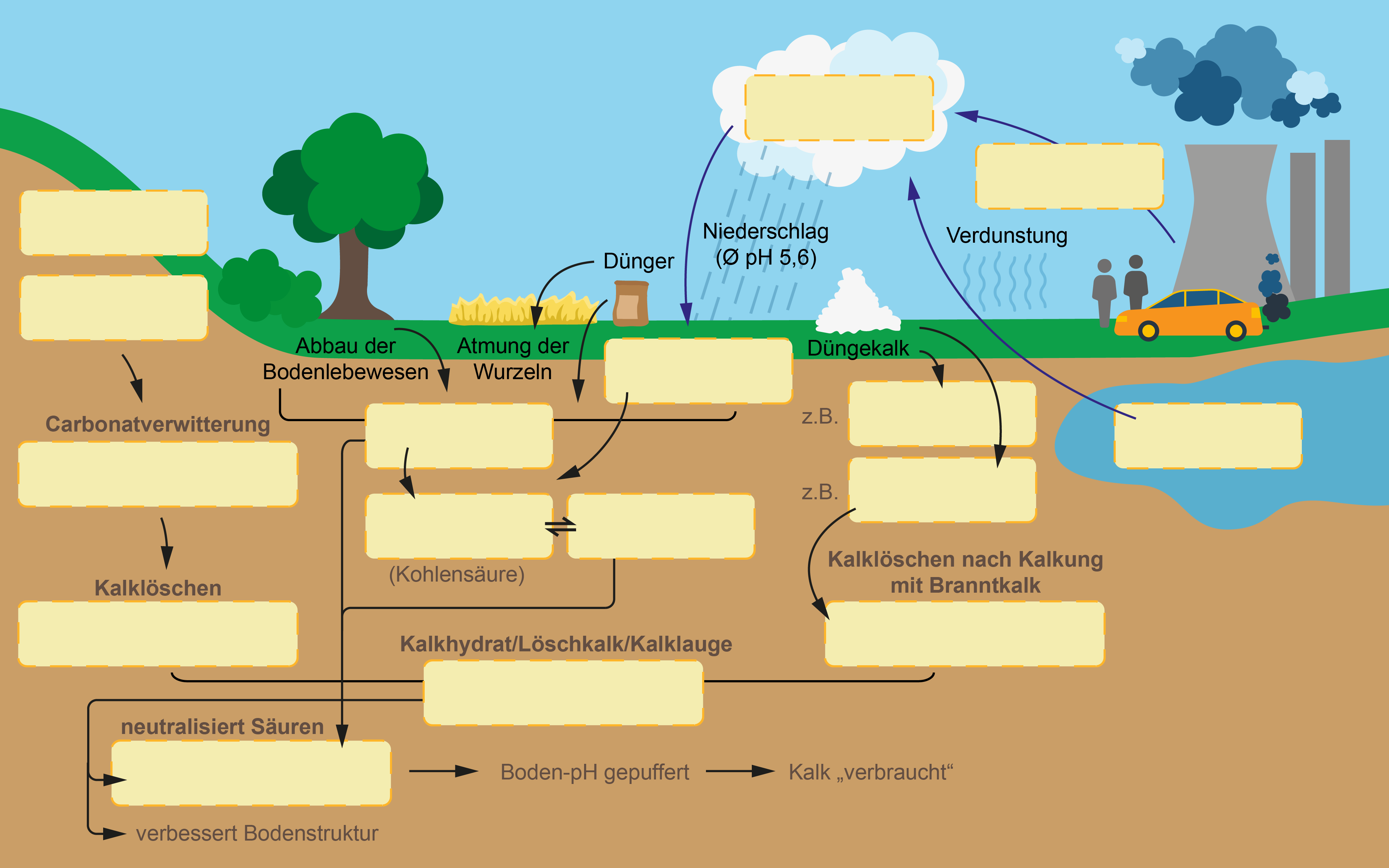
Kalk kommt von Natur aus als Gestein und in vielen Böden vor. Kalk besteht aus Calciumcarbonat (CaCO3) und teilweise Magnesiumcarbonat (MgCO3).
Bei der Lösung der chemischen Bindung des Carbonats liefert Kalk die Hydrogen-Ionen bzw. Basen (OH-), welche Bodensäuren (H+) abpuffern,
und andererseits Calcium-Ionen (Ca++). Die Ca++-Ionen spielen bei der Pufferung und Säureneutralisation keine Rolle, sind jedoch wesentlich,
um die Bodenstruktur zu verbessern (Tonflockung) und zu stabilisieren.
Im Detail läuft die Reaktion vom Kalk zu den Basen (OH-) über mehrere Stufen ab: Von Natur aus wird das Calciumcarbonat (CaCO3) im Boden durch
Kohlensäure aufgelöst. Die Kohlensäure (H2CO3) entsteht aus Wasser (H2O) und Kohlendioxid (CO2) in der Bodenluft, das Bodenlebewesen und
Pflanzenwurzeln bei ihrer Atmung und Umsetzung von organischer Substanz im Boden bilden.
Je aktiver das Bodenleben, desto stärker ist die CO2-Bildung, desto mehr Kohlensäure (H2CO3) fällt an. Diese löst das CaCO3
zu Calciumdihydrogencarbonat
Ca(HCO3)2, man spricht von der sog. Carbonatverwitterung. Aus dem Ca(HCO3)2 entsteht dann in Verbindung mit Wasser das
lösliche Calciumhydroxid [Ca(OH)2].
Die Reaktion heißt Kalklöschen. Erst das Ca(OH)2 bzw. die frei werdenden Hydrogen-Ionen (OH-) puffern die Bodensäuren (H+), wobei neutrales Wasser entsteht.
Bei einer Kalkung mit Branntkalk (CaO) entsteht in Verbindung mit Wasser sofort das Ca(OH)2, welches auch als Kalkhydrat, Kalkmilch, Carbidkalk oder
Kalklauge bezeichnet wird.
Kalk wirkt als Puffersystem für Säuren, die natürlich oder vom Menschen verursacht in den Boden gelangen, z. B. mit Niederschlägen: Regenwasser ist mit
einem durchschnittlichen pH von 5,6 schwach sauer, u. a. durch Verbrennungsabgase von Autos und Fabriken sowie Kohlensäure aus der Atmosphäre (saurer Regen = pH 4).
Weitere Säureeinträge können aus übermäßiger Düngung und Abbau von organischem Material stammen. Die Kalkpufferung ist von zentraler Bedeutung für einen stabilen
Boden-pH.
Ist der Boden von Natur aus kalkarm oder werden Kalkverluste nicht über Kalkungen ausgeglichen, versauert die Kohlensäure, die von den Bodenlebewesen produziert
wird, den Boden. Der pH-Wert im Boden sinkt ab. Erhöht sich hingegen die Konzentration an OH--Ionen, z. B. nach einer stärkeren Kalkung, werden H+-Ionen neutralisiert
(zu H2O), der Boden-pH steigt.